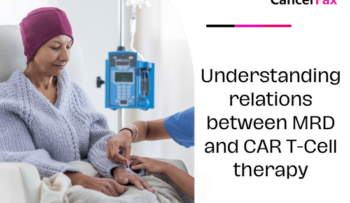
Comprendre les relations entre MRD et thérapie cellulaire CAR T
Qu’est-ce que le MRD dans le traitement du cancer ? La maladie résiduelle mesurable, ou MRD, est le nom désignant les très rares cellules cancéreuses qui restent dans le corps après ou pendant le traitement. Cytométrie en flux, réaction en chaîne par polymérase (PCR) ou nouvelle génération.
Thérapie par cellules souches mésenchymateuses dans les troubles neurologiques
Les maladies neurologiques constituent un problème majeur dans le monde entier car elles provoquent de nombreux décès et handicaps. Les traitements traditionnels n’ont pas toujours fonctionné, ce qui a conduit à une évolution vers de nouvelles méthodes telles que les thérapies cellulaires. Parce que..

La désignation de médicament orphelin est accordée par la FDA à CART T-Cell Therapy A2B530 pour le traitement du cancer colorectal
En mars 2024, un communiqué de presse indiquait que l'A2B530 (A2 Biotherapeutics), une thérapie cellulaire CAR T, avait reçu la désignation de médicament orphelin pour traiter le cancer colorectal qui exprime l'antigène carcinoembryonnaire (CEA) et a perdu l'expression HLA-A*02.
Amtagvi d'Iovance est approuvé par l'USFDA comme première thérapie par cellules T pour une tumeur solide
L'immunothérapie, la première du genre, d'Iovance Biotherapeutics a été approuvée par la FDA. Cela signifie que la thérapie par cellules T, qui a changé la façon dont certains types de cancer du sang sont traités, peut désormais être utilisée directement sur les tumeurs solides.
L'amivantamab-vmjw est approuvé par l'USFDA pour les indications du cancer du poumon non à petites cellules muté par insertion de l'exon 20 de l'EGFR
La Food and Drug Administration a approuvé l'amivantamab-vmjw (Rybrevant, Janssen Biotech, Inc.) en association avec le carboplatine et le pémétrexed le 1er mars 2024. Patients présentant une insertion de l'exon 20 du récepteur du facteur de croissance épidermique (EGFR).
L'osimertinib associé à la chimiothérapie est approuvé par l'USFDA pour le cancer du poumon non à petites cellules muté par EGFR
La Food and Drug Administration a approuvé l'osimertinib (Tagrisso, AstraZeneca Pharmaceuticals LP) en association avec une chimiothérapie à base de platine pour les patients atteints d'un cancer du poumon non à petites cellules localement avancé ou métastatique (la/mNSC).
Lifileucel est approuvé par l'USFDA pour le mélanome non résécable ou métastatique
La Food and Drug Administration a accordé une approbation accélérée au lifileucel (Amtagvi, Iovance Biotherapeutics, Inc.) le 16 février 2024. Cette approbation est destinée aux patients adultes atteints d'un mélanome non résécable ou métastatique qui ont été..
Le tépotinib est approuvé par l'USFDA pour le cancer du poumon non à petites cellules métastatique
La Food and Drug Administration a officiellement approuvé le tépotinib (Tepmetko, EMD Serono, Inc.) le 15 février 2024 pour les patients adultes atteints d'un cancer du poumon non à petites cellules (CPNPC) métastatique présentant une transition mésenchymateuse-épithéliale (M..
Le liposome d'irinotécan est approuvé par l'USFDA pour le traitement de première intention de l'adénocarcinome pancréatique métastatique
La Food and Drug Administration a approuvé le liposome d'irinotécan (Onivyde, Ipsen Biopharmaceuticals, Inc.) avec de l'oxaliplatine, du fluorouracile et de la leucovorine le 13 février 2024 pour le traitement de l'adénocarcinome pancréatique métastatique.
L'erdafitinib est approuvé par l'USFDA pour le carcinome urothélial localement avancé ou métastatique
L'erdafitinib (Balversa, Janssen Biotech) a été approuvé par la Food and Drug Administration le 19 janvier 2024 pour les patients adultes présentant des modifications génétiques FGFR3 qui sont atteints d'un carcinome urothélial localement avancé ou métastatique (mUC). Patie..