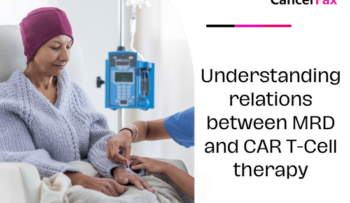
Izpratne par attiecībām starp MRD un CAR T-šūnu terapiju
What is MRD in cancer treatment? Measurable Residual Disease, or MRD, is the name for the very few cancer cells that stay in the body after or during treatment. Flow cytometry, polymerase chain reaction (PCR), or next-generati..
Mezenhimālo cilmes šūnu terapija neiroloģisku traucējumu gadījumā
Neurological diseases are big problems around the world because they cause a lot of death and disability. Traditional treatments haven't always worked, which has led to a change toward new methods like cell-based therapies. Beca..

Retu slimību ārstēšanai paredzēto zāļu apzīmējumu FDA ir piešķīrusi CART T-Cell Therapy A2B530 kolorektālā vēža ārstēšanai
In March 2024, a news release said that A2B530 (A2 Biotherapeutics), a CAR T-cell therapy, had been given Orphan Drug Designation to treat colorectal cancer that expresses carcinoembryonic antigen (CEA) and has lost HLA-A*02 expr..
USFDA ir apstiprinājusi Iovance Amtagvi kā pirmo T-šūnu terapiju cietam audzējam
Iovance Biotherapeutics' first-of-its-kind immunotherapy was approved by the FDA. This means that T-cell therapy, which has changed the way some types of blood cancer are treated, can now be used directly on solid tumors.The drug..
Amivantamab-vmjw ir apstiprinājusi USFDA EGFR eksona 20 ievietošanas mutācijas nesīkšūnu plaušu vēža indikācijām
The Food and Drug Administration approved amivantamab-vmjw (Rybrevant, Janssen Biotech, Inc.) in combination with carboplatin and pemetrexed on March 1, 2024. Patients with epidermal growth factor receptor (EGFR) exon 20 insertio..
Osimertinibu ar ķīmijterapiju ir apstiprinājusi USFDA EGFR mutācijas nesīkšūnu plaušu vēža ārstēšanai
The Food and Drug Administration approved osimertinib (Tagrisso, AstraZeneca Pharmaceuticals LP) in combination with platinum-based chemotherapy for patients with locally advanced or metastatic non-small cell lung cancer (la/mNSC..
Lifileucel ir apstiprinājusi USFDA nerezecējamas vai metastātiskas melanomas ārstēšanai
The Food and Drug Administration granted accelerated approval to lifileucel (Amtagvi, Iovance Biotherapeutics, Inc.) on February 16, 2024. This approval is for adult patients with unresectable or metastatic melanoma who have been..
USFDA ir apstiprinājusi tepotinibu metastātiska nesīkšūnu plaušu vēža ārstēšanai
The Food and Drug Administration officially approved tepotinib (Tepmetko, EMD Serono, Inc.) on February 15, 2024, for adult patients with metastatic non-small cell lung cancer (NSCLC) that had mesenchymal-epithelial transition (M..
Irinotekāna liposomu ir apstiprinājusi USFDA metastātiskas aizkuņģa dziedzera adenokarcinomas pirmās izvēles ārstēšanai
The Food and Drug Administration approved irinotecan liposome (Onivyde, Ipsen Biopharmaceuticals, Inc.) with oxaliplatin, fluorouracil, and leucovorin on February 13, 2024, for treating metastatic pancreatic adenocarcinoma as the..
Erdafitinibu ir apstiprinājusi USFDA lokāli progresējošas vai metastātiskas urotēlija karcinomas ārstēšanai
Erdafitinib (Balversa, Janssen Biotech) was approved by the Food and Drug Administration on January 19, 2024, for adult patients with FGFR3 genetic changes who have locally advanced or metastatic urothelial carcinoma (mUC). Patie..