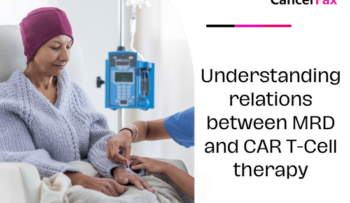
MRD- ja CAR-T-soluterapian välisten suhteiden ymmärtäminen
Mikä on MRD syövän hoidossa? Mitattavissa oleva jäännössairaus tai MRD on nimi niille harvoille syöpäsoluille, jotka pysyvät kehossa hoidon jälkeen tai sen aikana. Virtaussytometria, polymeraasiketjureaktio (PCR) tai seuraavat sukupolvet.
Mesenkymaalinen kantasoluhoito neurologisissa häiriöissä
Neurologiset sairaudet ovat suuria ongelmia ympäri maailmaa, koska ne aiheuttavat paljon kuolemia ja vammoja. Perinteiset hoidot eivät ole aina toimineet, mikä on johtanut muutokseen kohti uusia menetelmiä, kuten solupohjaisia hoitoja. Beca..

FDA on antanut harvinaislääkemerkinnän CART T-Cell Therapy A2B530:lle kolorektaalisyövän hoitoon
Maaliskuussa 2024 julkaistussa lehdistötiedotteessa kerrottiin, että A2B530 (A2 Biotherapeutics), CAR T-soluhoito, oli annettu harvinaislääkeluokitus karsinoembryonista antigeeniä (CEA) ilmentävän kolorektaalisyövän hoitoon ja että HLA-A*02 expr.
USFDA on hyväksynyt Iovancen Amtagvin ensimmäisenä T-soluhoitona kiinteään kasvaimeen
FDA hyväksyi Iovance Biotherapeuticsin ensimmäisen immunoterapian. Tämä tarkoittaa, että T-soluterapiaa, joka on muuttanut tapaa, jolla tietyntyyppisiä verisyöpätyyppejä hoidetaan, voidaan nyt käyttää suoraan kiinteisiin kasvaimiin.
USFDA on hyväksynyt amivantamab-vmjw:n EGFR-eksonin 20 insertiomutaation ei-pienisoluisen keuhkosyövän käyttöaiheisiin
Elintarvike- ja lääkevirasto hyväksyi amivantamab-vmjw:n (Rybrevant, Janssen Biotech, Inc.) yhdessä karboplatiinin ja pemetreksedin kanssa 1. maaliskuuta 2024. Potilaat, joilla on epidermaalisen kasvutekijäreseptorin (EGFR) eksoni 20 insertio.
Osimertinibi kemoterapian kanssa on USFDA:n hyväksymä EGFR-mutaation aiheuttaman ei-pienisoluisen keuhkosyövän hoitoon
Elintarvike- ja lääkevirasto hyväksyi osimertinibin (Tagrisso, AstraZeneca Pharmaceuticals LP) yhdessä platinapohjaisen kemoterapian kanssa potilaille, joilla on paikallisesti edennyt tai metastaattinen ei-pienisoluinen keuhkosyöpä (la/mNSC..
Lifileucel on USFDA:n hyväksymä ei-leikkauskelvoton tai metastaattinen melanooma
Elintarvike- ja lääkevirasto myönsi nopeutetun hyväksynnän lifileucelille (Amtagvi, Iovance Biotherapeutics, Inc.) 16. helmikuuta 2024. Tämä hyväksyntä on tarkoitettu aikuisille potilaille, joilla on leikkauskelvoton tai metastaattinen melanooma, jotka ovat...
USFDA on hyväksynyt tepotinibin metastaattisen ei-pienisoluisen keuhkosyövän hoitoon
Elintarvike- ja lääkevirasto hyväksyi tepotinibin (Tepmetko, EMD Serono, Inc.) virallisesti 15. helmikuuta 2024 aikuispotilaille, joilla on metastaattinen ei-pienisoluinen keuhkosyöpä (NSCLC), jolla oli mesenkymaali-epiteelimuutos (M..
Irinotekaaniliposomi on USFDA:n hyväksymä metastaattisen haiman adenokarsinooman ensilinjan hoitoon
Elintarvike- ja lääkevirasto hyväksyi irinotekaaniliposomin (Onivyde, Ipsen Biopharmaceuticals, Inc.) oksaliplatiinin, fluorourasiilin ja leukovoriinin kanssa 13. helmikuuta 2024 metastaattisen haiman adenokarsinooman hoitoon.
USFDA on hyväksynyt erdafitinibin paikallisesti edenneen tai metastaattisen uroteelisyövän hoitoon
Elintarvike- ja lääkevirasto hyväksyi erdafitinibin (Balversa, Janssen Biotech) 19. tammikuuta 2024 aikuispotilaille, joilla on FGFR3-geenimuutoksia ja joilla on paikallisesti edennyt tai metastaattinen uroteelisyöpä (mUC). Patie..