CAR T-Cell terapi til ikke-småcellet lungekræft
En revolutionerende tilgang til behandling af lungekræft.
Vil du tilmelde dig denne banebrydende kræftbehandling?
Marts 2024: CAR T-celleterapi er en potentiel kræftbehandlingsstrategi, især ved hæmatologiske maligniteter. Imidlertid er dets effektivitet i solide tumorer, såsom lungekræft, begrænset på grund af tumormikromiljøets immunsuppressive natur. Forskere udvikler næste generations CAR T-celler for at øge deres infiltration, overlevelse og persistens i maligne sygdomme. Kliniske forsøg er i gang for at vurdere sikkerheden og effektiviteten af CAR T-cellebehandlinger ved lungekræft, med nogle, der giver lovende resultater. Antigenflugt, immunologiske barrierer og on-target off-tumor skader er blandt udfordringerne i CAR T-celle behandling af lungekræft. Konstruktion af CAR-konstruktioner, ændring af tumormikromiljøet og anvendelse af CAR T-celler, der er tilgængelige fra hylden, er nogle strategier til at løse disse problemer.
Et af de førende hospitaler i Kina har med succes gennemført forsøg med CAR T-Cell-terapi hos ikke-småcellede lungekræftpatienter. CAR T-Cell på alle disse kræftformer er anvendelig for patienter efter nogle behandlingslinjer såsom operation, kemoterapi og strålebehandling, men med tilbagefald.
Af alle maligne sygdomme har lungekræft den største forekomst og dødelighed på verdensplan. Et voksende udvalg af immunoterapeutiske lægemidler, især dem, der retter sig mod monoklonale antistoffer, er blevet anvendt i den kliniske behandling af malignitet i den nuværende immunterapiperiode, selvom det stadig har adskillige ulemper. Ud over at blive brugt med succes mod hæmatologiske kræftformer, har kimære antigenreceptor-modificerede T (CAR-T)-celler også skabt nye muligheder for immunterapi af solide tumorer, såsom lungekræft. Manglen på passende tumorspecifikke antigener, et immunsuppressivt tumormikromiljø, et lavt niveau af CAR-T-cellepenetration i tumorvæv, sammen med off-target effekter osv. gør det vanskeligt at målrette mod lungekræftspecifikke antigener med modificeret CAR- T-celler. I mellemtiden er den kliniske brug af CAR-T-celler stadig begrænset på grund af adskillige vanskeligheder såsom tumorlysesyndrom, neurotoksicitetssyndrom og cytokinfrigivelsessyndrom. Med det mål at tilbyde friske perspektiver og metoder til prækliniske undersøgelser og kliniske forsøg med CAR-T-celleterapi for lungekræft, skitserer vi den grundlæggende struktur og generationskarakteristika for CAR-T-celler i denne gennemgang, opsummerer de typiske tumorassocierede antigener, og fremhæve de aktuelle udfordringer.
Strukturen af BILER
Siden starten har brugen af CAR'er i T-celleterapi gennemgået fire iterative generationer, som alle er baseret på CAR'ens intracellulære signaldomæner. Den første generation af CAR'er havde svag aktivitet og en kort in vivo overlevelsestid, fordi de kun indeholdt antigengenkendelsessignalet. Signaltransduktionsområdet for henholdsvis anden og tredje generations CAR'er indeholdt et og to costimulerende molekyler. Disse ændringer blev foretaget for at øge T-celleoverlevelse, cytotoksicitet og proliferation. De co-stimulerende molekyler i CAR'erne blev forbedret, hvilket forbedrede CAR-T-cellernes ydeevne. 4-1BB eller CD28 er de to andengenerations co-stimulerende domæner, der oftest anvendes. Derudover er cytotoksicitet, cytokinproduktion og T-celleaktivering alle blevet påvist at blive forbedret af DNAX-aktiverende protein 10 (DAP10). Baseret på ikke-småcellet lungecancer (NSCLC) cellelinjer blev forsinket initial lungecancervækst og øget antitumoraktivitet påvist i in vivo dyremodeller af human lungecancer xenotransplantation. Pro-inflammatoriske cytokiner og co-stimulerende ligander blev tilføjet i fjerde generations CAR-T design for at hjælpe T-cellerne med at infiltrere og komme ud over den fjendtlige TME's undertrykkende egenskaber.
Amplifikation og antitumoreffektivitet af CAR-T-celler er blevet påvist at blive forbedret ved at forbedre den ekstracellulære modulstruktur ud over intracellulære signaltransduktionsmoduler. Ifølge Qin et al., blev det enkeltkædede variable fragment (scFv), som binder til og tilskynder til ekspansion, migration og invasion af cluster of differentiation 4 (CD4)+ CAR-T-celler, gjort mere fleksibelt ved tilføjelsen af en hængselstruktur. Selvom andengenerations CAR-T-celler fortsat er standardmetoden til terapeutisk anvendelse, bliver CAR'ernes strukturelle arkitektur konstant forbedret og er afgørende for CAR-effektiviteten. T's
CAR T-Cell terapi ved lungekræft og målantigen
Når target-antigenet udelukkende udtrykkes på cancerceller eller er overudtrykt på alle eller størstedelen af lungecancerceller i sammenligning med normale celler, er dette det bedste mål for CAR-T-cellebehandling. Selvom et stort antal tumorassocierede antigener (TAA) er blevet fundet i ikke-småcellet lungecancer (NSCLC), er kun nogle få af disse antigener blevet specifikt målrettet af CAR-T-celler (8). Derudover er nogle af disse mål-antigener også svagt udtrykt i sundt væv, hvilket giver nogle CAR-T-celler evnen til at angribe raske celler.
Epidermal vækstfaktorreceptor (EGFR), human epidermal vækstfaktorreceptor 2 (HER2), mesothelin (MSLN), prostatastamcelleantigen (PSCA), mucin 1 (MUC1), carcinoembryonalt antigen (CEA), tyrosinkinase-lignende forældreløs receptor ( ROR1), programmeret dødsligand 1 (PD-L1) og CD80/CD86 er blandt de mål, der i øjeblikket studeres for CAR.
Lungekræftpatient i CAR T-cellebehandling
november 2009 fandt patienten en venstre lungemasse og gennemgik radikal venstre lungekræft radikal operation. Patologi: lungeadenokarcinom;
Fra jan 2013 til jan 2017 opstod tre hjernemetastaser, og operation og strålebehandling blev givet successivt med dårlig kontrol;
Fra marts 2017 til september 2017 blev der til hjernemetastaser givet mesoCAR-αPD1-celler, der udtrykker PD-1-antistof, til 6 behandlingsforløb. Efter behandling blev PR vurderet, og tumorer faldt signifikant med kun en lille mængde rest.
BIL T-cellebehandling i Kina
CAR-T celleterapi i Kina vokser i et meget hurtigt tempo. Resultater af CAR T-celleterapi i Kina og den samlede helbredelsesrate er blandt de bedste i verden på nuværende tidspunkt. Der er mere end 300 kliniske forsøg, der finder sted i Kina til CAR T-celleterapi. Kina er blandt de første lande, der tilbyder CAR T-celleterapi efter USA & UK. Med hensyn til antallet af kliniske CAR-T-forsøg ligger Kina næst efter USA og registrerer cirka 33 % af forsøgene på verdensplan. Antallet af CAR T-cellebehandlinger i klinisk udvikling er steget voldsomt i de seneste år. I øjeblikket er der i Kina over 300 igangværende kliniske forsøg med hæmatologiske maligniteter såvel som solide tumorer.
China’s extensive explorations and breakthroughs in the search of novel target antigens, optimization of CAR structure, cocktail CAR-T therapy, combination therapy, and extension of CAR-T cell applications, imply that we are currently on the verge of a revolution in CAR-T therapy. US FDA has approved CAR T Celleterapi for relapsed B Acute lymphoblastic leukemia, lymphoma & multiple myeloma. Kina har for nylig godkendt CAR T-Cell-terapi til nogle solide kræftformer. Patienter fra hele verden vil sandsynligvis drage fordel af denne udvikling.
Du kan godt lide at læse: BIL T-cellebehandling i Kina
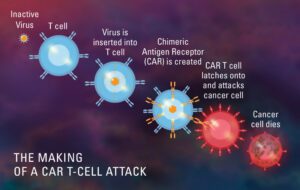
Hvad er CAR T-celleterapi (kimære antigenreceptorer)?
CAR T-celleterapi er en form for immunterapi, der bruger specielt modificerede T-celler, som er en del af vores immunsystem til at bekæmpe kræft. En prøve af patienters T-celler opsamles fra blodet, hvorefter den modificeres til at producere specielle strukturer kaldet kimære antigenreceptorer (CAR) på deres overflade. Når disse modificerede CAR-celler geninfunderes i patienten, angriber disse nye celler det specifikke antigen og dræber tumorcellerne.
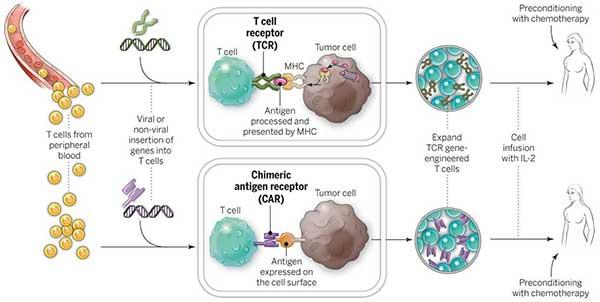
Hvordan fungerer CAR T-celleterapi?
CAR T-cell therapy takes help from body’s own immune system to attack and kill cancer cells. This is done by removing some specified cells from the blood of the patient, modifying them in the lab and re-injecting them into the patient. CAR T-cell therapy has produced very encouraging results in Non-Hodgkin lymphoma and thus approved by FDA.
Hvem er de rigtige kandidater til CAR T-Cell-terapi?
På nuværende tidspunkt har FDA godkendt CAR T-cellebehandling til nogle former for aggressivt og refraktært non-Hodgkin lymfom og recidiverende og refraktær akut lymfatisk leukæmi. Patienten skal sende fuldstændige lægerapporter for at fastslå brugen af CAR T-Cell-terapi til sin behandling.
Inklusionskriterier for CAR T-cellebehandling:
1. Patienter med CD19+ B-celle lymfom (mindst 2 tidligere kombinationskemoterapiregimer)
2. At være i alderen 3 til 75 år
3. ECOG-score ≤2
4. Kvinder i den fertile alder skal have taget en uringraviditetstest og være negativ før behandlingen. Alle patienter accepterer at bruge pålidelige præventionsmetoder i løbet af forsøgsperioden og indtil opfølgning for sidste gang.
Eksklusionskriterier for CAR T-cellebehandling:
1. Intrakraniel hypertension eller bevidstløshed
2. Åndedrætssvigt
3. Dissemineret intravaskulær koagulation
4. Hæmatosepsis eller ukontrolleret aktiv infektion
5. Ukontrolleret diabetes
Fordele ved CAR T-celleterapi
- > 5000 CAR T-sager udført af højt kvalificerede læger.
- Hospitaler i Kina har udviklet flere CAR T-celletyper inklusive CD19 & CD 22 end ethvert andet land i verden.
- Kina gennemfører mere end 300 kliniske forsøg med CAR T-celleterapi. Mere end noget andet land på planeten.
- Den kliniske effekt af CAR T Cell ligner den i USA eller ethvert andet land og undertiden bedre.
Behandlingsproces for CAR T-celleterapi
- Komplet evaluering af patienten
- T-celleopsamling fra kroppen
- T-celler konstrueres derefter i laboratoriet
- Genmodificerede T-celler ganges derefter ved at bruge dem til at dyrke i laboratoriet. Disse celler nedfryses og sendes derefter til behandlingscentre.
- Før infusion kan patienten få kemoterapi for deres kræft. Dette hjælper terapien med at arbejde bedre.
- Kort efter kemoterapi inficeres CAR T-celler ved en proces, der ligner blodinfusion.
- Der er en 2-3 måneders restitutionsperiode for patienten.
Tidsramme for CAR T-celleterapi
1. Eksamen og test: en uge
2. Forbehandling & T-celleopsamling: en uge
3. T-celleforberedelse og retur: to-tre uger
4. 1. effektivitetsanalyse: tre uger
5. 2. effektivitetsanalyse: tre uger.
Bivirkninger af CAR T-celleterapi
De almindelige bivirkninger af CAR T-cellebehandling inkluderer:
- Cytokinfrigivelsessyndrom
I nogle tilfælde kan patienter udvikle influenzalignende symptomer såsom feber, kulderystelser, hovedpine, kvalme, opkastning, løs afføring og muskel- eller ledsmerter. Det kan også forårsage lavt blodtryk, åndedrætsbesvær og en hurtig puls. Disse bivirkninger skyldes frigivelsen af cytokiner fra immuncellerne under CAR T-cellebehandling. Disse symptomer er normalt milde, men kan være alvorlige og livstruende hos nogle patienter. - Neurologiske hændelser
Neurologiske hændelser kan forekomme og kan være alvorlige hos nogle patienter. Sådanne hændelser inkluderer encefalopati (hjerneskade og funktionsfejl), forvirring, vanskeligheder med at tale, agitation, kramper, døsighed, ændret bevidsthedstilstand og tab af balance. - Neutropeni og anæmi
Nogle patienter kan udvikle neutropeni eller lavt antal hvide blodlegemer. På samme måde kan anæmi eller lavt antal røde blodlegemer også forekomme på grund af denne terapi.
.
Heldigvis forsvinder de fleste af disse bivirkninger normalt af sig selv eller kan håndteres ved brug af medicin.
Hvor effektiv er CAR T-celleterapi?
CAR T-celleterapi til behandling af lymfom og andre blodkræftformer har vist lovende resultater. Siden CAR T-cellebehandling havde mange patienter, der tidligere havde tilbagefald, blodtumorer lovende resultater og ingen tegn på kræft. Det har også hjulpet til rehabilitering af patienter, der tidligere ikke har reageret på de fleste traditionelle kræftterapier.
Imidlertid er der behov for længerevarende undersøgelser for en større patientpopulation for at validere effektiviteten af denne behandling. Store eksperimenter vil også hjælpe med at bestemme sandsynligheden for bivirkninger og de rigtige måder at håndtere dem på.
Hvor meget koster CAR T-celleterapi?
Kina er en af verdens førende inden for CAR-T-celleterapi og BMT. Indtil nu er der mere end 300 CAR-T-celle kliniske forsøg i gang. Kinas CAR-T-behandling er den mest budgetvenlige i verden. Fordi CAR-T-celleforberedelsen er gratis nu! Patienterne skal kun betale for behandlingen og ydelserne. Samlede behandlingsomkostninger vil være omkring $60,000 - $80,000.
Læs også dette: CAR T Celleterapi i Indien
Hvordan kan jeg tage CAR T-Cell-terapi i Kina?
Patienten kan ringe til +91 96 1588 1588 eller e-maile til cancerfax@gmail.com med patientoplysninger og medicinske rapporter, og vi sørger for second opinion, behandlingsplan og skøn over udgifter.