CAR T-Cell terápia nem kissejtes tüdőrák kezelésére
Forradalmi megközelítés a tüdőrák kezelésében.
Szeretnél beiratkozni ebbe az áttörő rákkezelésbe?
March 2024 : CAR T-cell therapy is a potential cancer treatment strategy, notably in hematological malignancies. However, its effectiveness in solid tumors, such as lung cancer, is limited due to the tumor microenvironment’s immunosuppressive nature. Researchers are developing next-generation CAR T cells to boost their infiltration, survival, and persistence inside malignancies. Clinical trials are underway to assess the safety and efficacy of CAR T-cell treatments in lung cancer, with some yielding promising results. Antigen escape, immunological barriers, and on-target off-tumor damage are among the challenges in CAR T-cell treatment for lung cancer. Engineering CAR constructs, altering the tumor microenvironment, and employing off-the-shelf CAR T cells are some strategies for addressing these problems.
One of the leading hospitals in China has successfully conducted trials of CAR T-Cell therapy in nem kissejtes tüdőrák patients. CAR T-Cell on all these cancers is applicable for patients after some lines of treatment such as surgery, chemotherapy and radiotherapy but relapsed.
Of all malignancies, lung cancer has the greatest incidence and fatality rates worldwide. A growing variety of immunotherapeutic medicines, particularly those that target monoclonal antibodies, have been employed in the clinical treatment of malignancy in the current immunterápia period, although it still has numerous drawbacks. In addition to being utilised successfully against haematological cancers, chimeric antigen receptor-modified T (CAR-T) cells have also created new opportunities for the immunotherapy of solid tumours, such as lung cancer. The lack of appropriate tumor-specific antigens, an immunosuppressive tumour microenvironment, a low level of CAR-T cell penetration into tumour tissues, together with off-target effects, etc. make it difficult to target tüdőrák-specific antigens with modified CAR-T cells. Meanwhile, due to numerous difficulties such as tumor lysis syndrome, neurotoxicity syndrome, and citokin felszabadulás szindróma, the clinical usage of CAR-T cells is still restricted. With the goal of offering fresh perspectives and methods for pre-clinical studies and clinical trials of CAR-T cell therapy for lung cancer, we outline the fundamental structure and generation characteristics of CAR-T cells in this review, summarise the typical tumor-associated antigens, and highlight the current challenges.
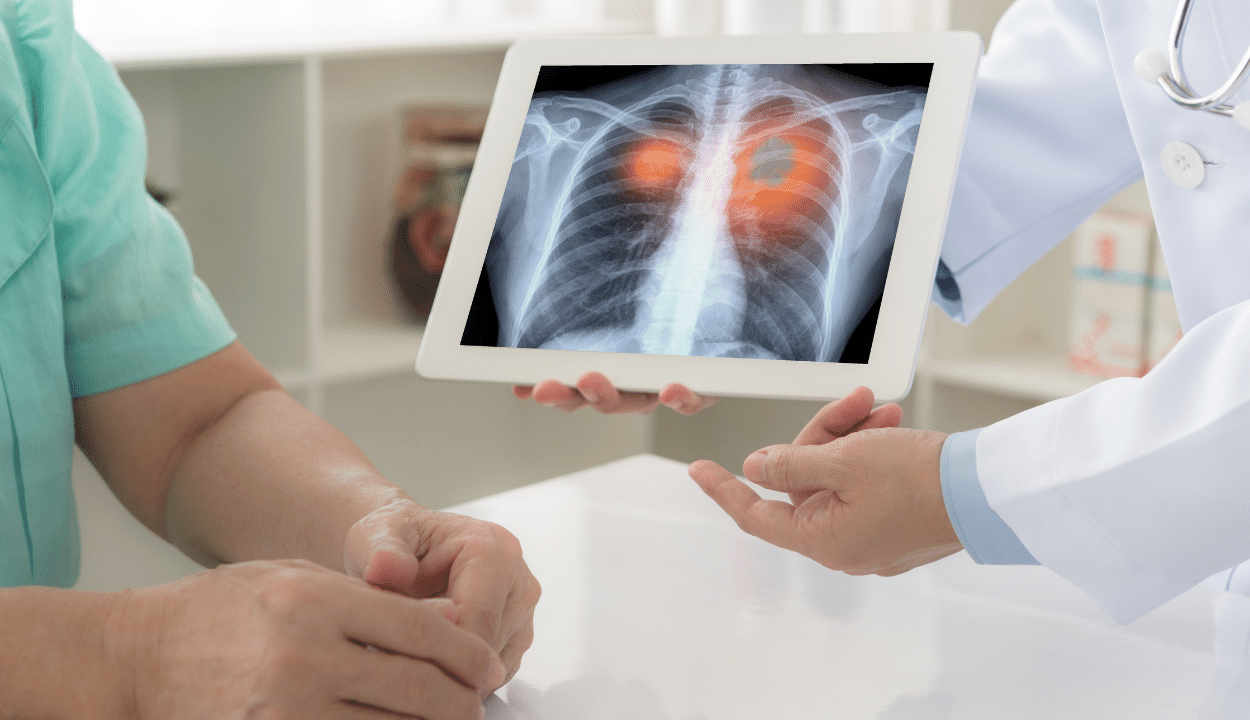
A CARS felépítése
Megalakulása óta a CAR-ok T-sejtterápiában történő alkalmazása négy iteratív generáción keresztül ment keresztül, amelyek mindegyike a CAR intracelluláris szignáldoménjein alapul. A CAR-ok első generációja gyenge aktivitással és rövid in vivo túlélési idővel rendelkezett, mivel csak az antigénfelismerő jelet tartalmazták. A második és harmadik generációs CAR jelátviteli területe egy, illetve két kostimuláló molekulát tartalmazott. Ezeket a változtatásokat a T-sejtek túlélésének, citotoxicitásának és proliferációjának növelése érdekében hajtották végre. A CAR-okban lévő kostimuláló molekulák javultak, ami javította a CAR-T sejtek teljesítményét. A 4-1BB vagy a CD28 a két leggyakrabban használt második generációs kostimuláló domén. Ezenkívül kimutatták, hogy a citotoxicitás, a citokintermelés és a T-sejt aktiváció mind javítja a DNSX-aktiváló 10-es fehérjét (DAP10). A nem-kissejtes tüdőrák (NSCLC) sejtvonalak alapján a tüdőrák kezdeti késleltetett növekedését és megnövekedett daganatellenes aktivitását mutatták ki humán tüdőrák xenotranszplantációjának in vivo állatmodelljeiben. Pro-inflammatorikus citokineket és kostimuláló ligandumokat adtunk a negyedik generációs CAR-T tervezéshez, hogy segítsék a T-sejtek beszivárgását, és túllépjenek az ellenséges TME elnyomó tulajdonságain.
Kimutatták, hogy a CAR-T sejtek amplifikációja és daganatellenes hatékonysága fokozódik az extracelluláris modul szerkezetének javításával az intracelluláris jelátviteli modulok mellett. Qin és munkatársai szerint az egyláncú variábilis fragmenst (scFv), amely a differenciálódási 4 (CD4)+ CAR-T sejtek klaszteréhez kötődik, és elősegíti azok expanzióját, migrációját és invázióját, rugalmasabbá tették a hozzáadással. egy csuklós szerkezetről. Bár a második generációs CAR-T sejtek továbbra is a terápiás alkalmazás szokásos módszerei, a CAR-ok szerkezeti felépítése folyamatosan javul, és ez kulcsfontosságú a CAR hatékonysága szempontjából. T's
CAR T-sejt terápia tüdőrákban és célantigén
Ha a cél-antigén kizárólag a rákos sejteken expresszálódik, vagy a tüdőráksejtek egészén vagy többségén túlzottan expresszálódik a normál sejtekhez képest, ez a legjobb célpont a CAR-T-sejt-kezeléshez. Bár nagyszámú tumor-asszociált antigént (TAA) találtak a nem-kissejtes tüdőrákokban (NSCLC), ezek közül csak néhány antigént céloznak meg kifejezetten a CAR-T-sejtek (8). Ezen túlmenően ezen célantigének némelyike az egészséges szövetekben is gyengén expresszálódik, így egyes CAR-T-sejtek képesek megtámadni az egészséges sejteket.
Epidermális növekedési faktor receptor (EGFR), humán epidermális növekedési faktor receptor 2 (HER2), mezotelin (MSLN), prosztata őssejt antigén (PSCA), mucin 1 (MUC1), karcinoembrionális antigén (CEA), tirozin kináz-szerű árva receptor ( A ROR1), a programozott halál ligandum 1 (PD-L1) és a CD80/CD86 a CAR jelenleg vizsgált célpontjai közé tartoznak.
Tüdőrákos beteg, aki CAR T-sejtes terápiában részesül
2009 novemberében a beteg bal tüdőtömeget talált, és radikális bal tüdőrák radikális műtéten esett át. Patológia: tüdő adenokarcinóma;
2013 januárja és 2017 januárja között három agyi áttét fordult elő, és a műtétet és a sugárterápiát egymás után végezték rossz kontroll mellett;
2017 márciusától 2017 szeptemberéig az agyi áttétek esetében a PD-1 antitestet expresszáló mezoCAR-αPD1 sejteket 6 kezelésig adták. A kezelés után a PR-t értékelték, és a daganatok jelentősen zsugorodtak, csak kis mennyiségű maradékkal.
CAR T-sejt terápia Kínában
CAR-T sejtterápia Kínában nagyon gyors ütemben növekszik. Eredményei CAR T-sejtterápia Kínában és az általános gyógyulási arány jelenleg a világ legjobbjai közé tartozik. Jelenleg több mint 300 klinikai vizsgálat zajlik Kína CAR T sejtterápiához. Kína az elsők között kínálja a CAR T sejt terápiát USA & UK. A CAR-T klinikai vizsgálatok számát tekintve Kína a második az Egyesült Államok után, a világszerte végzett vizsgálatok hozzávetőleg 33%-át regisztrálva. A klinikai fejlesztés alatt álló CAR T-sejtes terápiák száma az elmúlt években rohamosan megugrott. Jelenleg Kínában több mint 300 klinikai vizsgálat folyik hematológiai rosszindulatú daganatok, valamint szolid daganatok terén.
China’s extensive explorations and breakthroughs in the search of novel target antigens, optimization of CAR structure, cocktail CAR-T therapy, combination therapy, and extension of CAR-T cell applications, imply that we are currently on the verge of a revolution in CAR-T therapy. US FDA has approved CAR T sejtterápia for relapsed B Acute lymphoblastic leukemia, lymphoma & multiple myeloma. Kína a közelmúltban jóváhagyta a CAR T-Sejt terápiát néhány szilárd rák esetében. Valószínűleg a világ minden tájáról származó betegek profitálnak ebből a fejlesztésből.
Érdemes elolvasni: CAR T-sejt terápia Kínában
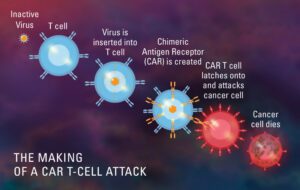
Mi a CAR T-sejt terápia (kiméra antigén receptorok)?
A CAR T-Cell terápia az immunterápia egyik formája, amely speciálisan módosított T-sejteket használ, amelyek immunrendszerünk részét képezik a rák elleni küzdelemben. A betegek véréből mintát gyűjtenek a T-sejtekből, majd úgy módosítják, hogy speciális struktúrákat, úgynevezett kiméra antigén receptorokat (CAR) hozzon létre a felületükön. Amikor ezeket a módosított CAR sejteket újra beadják a páciensbe, ezek az új sejtek megtámadják a specifikus antigént és elpusztítják a daganatsejteket.
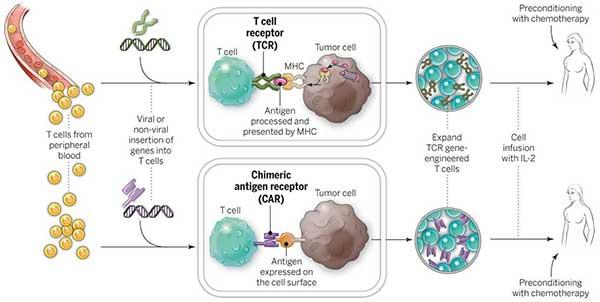
Hogyan működik a CAR T-Cell terápia?
A CAR T-sejt terápia a szervezet saját immunrendszerének segítségét veszi igénybe, hogy megtámadja és elpusztítsa a rákos sejteket. Ez úgy történik, hogy eltávolítanak bizonyos sejteket a páciens véréből, módosítják azokat a laboratóriumban, és újra befecskendezik a betegbe. A CAR T-sejt terápia nagyon biztató eredményeket hozott Nem Hodgkin limfóma és így az FDA jóváhagyta.
Kik a megfelelő jelöltek a CAR T-Cell terápiára?
At present FDA has approved CAR T-Cell therapy for some forms of aggressive and refractory Non-Hodgkin lymphoma and relapsed and refractory akut limfoblasztikus leukémia. A betegnek teljes körű orvosi jelentést kell küldenie, hogy megbizonyosodjon arról, hogy a CAR T-Cell terápiát használják-e kezelésében.
A CAR T-sejtes terápia felvételi kritériumai:
1. CD19+ B-sejtes limfómában szenvedő betegek (legalább 2 korábbi kombinált kemoterápiás kezelés)
2. 3–75 évesnek lenni
3. ECOG pontszám ≤2
4. Fogamzóképes korú nőknél terhességi vizeletvizsgálatot kell végezni, amely negatívnak bizonyult a kezelés előtt. Minden beteg beleegyezik abba, hogy megbízható fogamzásgátlási módszereket alkalmaz a próbaidőszak alatt és az utolsó vizsgálatig.
Kizárási kritériumok a CAR T-sejtes terápiához:
1. Koponyaűri magas vérnyomás vagy eszméletvesztés
2. Légzési elégtelenség
3. Disszeminált intravaszkuláris koaguláció
4. Hematosepsis vagy kontrollálatlan aktív fertőzés
5. Nem kontrollált cukorbetegség
A CAR T-Cell terápia előnyei
- > 5000 CAR T esetet magasan képzett orvosok végeznek.
- A kínai kórházak több CAR T-sejt-típust fejlesztettek ki, köztük a CD19 és CD 22-et, mint a világ bármely más országában.
- Kína több mint 300 klinikai vizsgálatot végez a CAR T sejtterápián. Több, mint bármely más ország a bolygón.
- A CAR T sejt klinikai hatása hasonló az USA-ban vagy bármely más országban tapasztalhatóhoz, és néha jobb.
A CAR T-Cell terápia kezelési folyamata
- A páciens teljes értékelése
- T-sejtgyűjtés a testből
- A T-sejteket ezután a laboratóriumban megtervezzük
- A genetikailag módosított T-sejteket ezután a laboratóriumban történő növesztéssel megsokszorozzák. Ezeket a sejteket lefagyasztják, majd a kezelő központokba küldik.
- Az infúzió beadása előtt a beteg kemoterápiát kaphat rákja miatt. Ez segíti a terápia jobb működését.
- A kemoterápia után nem sokkal a CAR T-sejteket olyan infúzióval infundálják, amely hasonló a vérinfúzióhoz.
- Van egy 2-3 hónapos gyógyulási időszak a beteg számára.
Időkeret a CAR T-Cell terápiához
1. Vizsgálat és teszt: egy hét
2. Előkezelés és T-sejt-gyűjtés: egy hét
3. T-sejt előkészítés és visszatérés: két-három hét
4. 1. Hatékonyságelemzés: három hét
5. 2. Hatékonysági elemzés: három hét.
A CAR T-Cell terápia mellékhatásai
A CAR T-sejt terápia gyakori mellékhatásai a következők:
- Citokin felszabadulási szindróma
Egyes esetekben a betegeknél influenzaszerű tünetek jelentkezhetnek, például láz, hidegrázás, fejfájás, hányinger, hányás, laza széklet, valamint izom- vagy ízületi fájdalmak. Alacsony vérnyomást, légzési nehézséget és gyors szívverést is okozhat. Ezek a mellékhatások az immunsejtek által a CAR T-sejtes terápia során felszabaduló citokinek következményei. Ezek a tünetek általában enyhék, de egyes betegeknél súlyosak és életveszélyesek is lehetnek. - Neurológiai események
Neurológiai események előfordulhatnak, és egyes betegeknél súlyosak lehetnek. Ilyen események lehetnek az encephalopathia (agysérülés és működési zavar), zavartság, beszédzavar, izgatottság, görcsrohamok, álmosság, megváltozott tudatállapot és egyensúlyvesztés. - Neutropenia és vérszegénység
Egyes betegeknél neutropenia vagy alacsony fehérvérsejtszám alakulhat ki. Hasonlóképpen vérszegénység vagy alacsony vörösvérsejtszám is előfordulhat ennek a terápiának köszönhetően.
.
Szerencsére ezeknek a mellékhatásoknak a többsége általában magától megszűnik, vagy gyógyszeres kezeléssel kezelhető.
Mennyire hatékony a CAR T-Cell terápia?
CAR T-sejt terápia kezelésére lymphoma és más vérrákok ígéretes eredményeket mutattak. A CAR T-sejtes kezelés óta sok olyan beteg, aki korábban visszaesett a vértumorok ígéretes eredményekkel jártak, és nem mutattak rá bizonyítékot. Segített azoknak a betegeknek a rehabilitációjában is, akik korábban nem reagáltak a legtöbb hagyományos rákterápiára.
A kezelés hatékonyságának igazolásához azonban hosszabb távú vizsgálatokra van szükség nagyobb betegcsoport számára. A nagyszabású kísérletek szintén segítenek meghatározni a mellékhatások valószínűségét és a kezelésük helyes módjait.
Mennyibe kerül az CAR T-Cell terápia?
Kína világelső a CAR-T sejtterápia és a BMT területén. Jelenleg több mint 300 CAR-T sejtes klinikai vizsgálat van folyamatban. A kínai CAR-T kezelés a legköltségesebb a világon. Mert a CAR-T sejt előkészítés most ingyenes! A betegeknek csak a kezelésért és a szolgáltatásokért kell fizetniük. A kezelés teljes költsége körülbelül 60,000 80,000-XNUMX XNUMX dollár lesz.
Olvassa el ezt is: CAR T sejtterápia Indiában
Hogyan szedhetem az CAR T-Cell terápiát Kínában?
A páciens a +91 96 1588 1588-as telefonszámon vagy a cancerfax@gmail.com e-mail címen küldheti el a páciens adatait és az orvosi jelentéseket, és megbeszéljük a második véleményt, a kezelési tervet és a költségbecslést.